Hóa học 10 Bài 19: Luyện tập Phản ứng oxi hóa - khử Giải bài tập Hóa 10 trang 88, 89, 90
Giải Hóa 10 Bài 19 giúp các em học sinh lớp 10 nắm vững được kiến thức về sự oxi hóa, sự khử, chất oxi hóa, chất khử, phản ứng oxi hóa khử. Đồng thời giải nhanh được các bài tập Hóa học 10 chương IV trang 88, 89, 90.
Giải bài tập Hóa 10 bài 19 trước khi đến lớp các em nhanh chóng nắm vững kiến thức hôm sau ở trên lớp sẽ học gì, hiểu sơ qua về nội dung học. Đồng thời giúp thầy cô tham khảo, nhanh chóng soạn giáo án cho học sinh của mình. Vậy sau đây là nội dung chi tiết tài liệu, mời các bạn cùng tham khảo tại đây.
Hóa 10 bài 19: Luyện tập Phản ứng oxi hóa - khử
Giải bài tập SGK Hóa 10 trang 88, 89, 90
Câu 1
Loại phản ứng nào sau đây luôn luôn không là loại phản ứng oxi hóa - khử?
A. Phản ứng hóa hợp.
B. Phản ứng phân hủy.
C. Phản ứng thế trong hóa vô cơ
D. Phản ứng trao đổi.
Gợi ý đáp án
D đúng.
Câu 2
Loại phản ứng nào sau đây luôn luôn là phản ứng oxi hóa - khử?
A. Phản ứng hóa hợp.
B. Phản ứng phân hủy.
C. Phản ứng thế trong hóa vô cơ.
D. Phản ứng trao đổi.
Gợi ý đáp án
C đúng.
Câu 3
Cho phản ứng: M2Ox + HNO3 → M(NO3)2 + ...
Khi x có giá trị là bao nhiêu thì phản ứng trên không thuộc loại phản ứng oxi hóa - khử?
A. x = 1.
B. x = 2.
C. x= 1 hoặc x = 2.
D. x = 3.
Chọn đáp án đúng.
Gợi ý đáp án
D đúng.
Câu 4
Câu nào đúng, câu nào sai trong các câu sau đây:
A. Sự oxi hóa một nguyên tố là lấy bớt electron của nguyên tố đó, là làm cho số oxi hóa của nguyên tố đó tăng lên.
B. Chất oxi hóa là chất thu electron, là chất chứa nguyên tố mà số oxi hóa của nó tăng sau phản ứng.
C. Sự khử một nguyên tố là sự thu thêm electron cho nguyên tố đó, làm cho số oxi hóa của nguyên tố đó giảm xuống.
D. Chất khử là chất thu electron, là chất chứa nguyên tố mà số oxi hóa của nó giảm sau phản ứng.
E. Tất cả đều sai
Gợi ý đáp án
Câu sai: B, D.
Câu đúng: A, C.
Câu 5
Hãy xác định số oxi hóa của các nguyên tố:
Nitơ trong NO, NO2, N2O5, HNO3, HNO2, NH3, NH4Cl.
Clo trong HCl, HClO, HClO2, HClO3, HClO4, CaOCl2.
Mangan trong MnO2, KMnO4, K2MnO4, MnSO4.
Crom trong K2Cr2O7, Cr2(SO4)3, Cr2O3.
Lưu huỳnh trong H2S, SO2, H2SO3, H2SO4, FeS, FeS2.
Gợi ý đáp án
Đặt x là oxi hóa của nguyên tố nitơ trong các hợp chất trên, ta có:
Trong NO: x + (-2) = 0 → x = +2.
Trong NO2: x + 2(-2) = 0 → x = +4.
Trong N2O5: 2x + 5(-2) = 0 → x = +5.
Trong HNO3: (+1) +x + 3(-3) = 0 → x = +5.
Trong HNO2: (+1) + x +2(-2) = 0 → x = +3.
Trong NH3: x + 3(+1) = 0 → x = -3.
Trong NH3Cl: x + 4(+1) +(-1) = 0 → x = -3.
Cũng giải tương tự như trên ta có:

Câu 6
Cho biết đã xảy ra sự oxi hóa và sự khử những chất nào trong những phản ứng thế sau:
a) Cu + 2AgNO3 → Cu(NO3)2 + 2Ag.
b) Fe + CuSO4 → FeSO4 + Cu.
c) 2Na + 2H2O → 2NaOH + H2.
Gợi ý đáp án
Sự oxi hóa và sự khử những chất trong phản ứng thế sau:
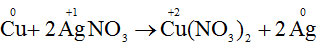
Sự nhường electron của Cu được gọi là sự oxi hóa nguyên tử đồng.
Sự nhận electron của ion bạc được gọi là sự khử ion bạc.
![]()
Sự nhường electron của sắt được gọi là sự oxi hóa nguyên tử sắt.
Sự nhận electron của ion đồng được gọi là sự khử ion đồng.
![]()
Sự nhường electron của natri được gọi là sự oxi hóa nguyên tử natri.
Sự nhận electron của ion hidro gọi là sự khử ion hiđro.
Câu 7
Dựa vào sự thay đổi số oxi hóa, tìm chất oxi hóa và chất khử trong những phản ứng sau:
a) 2H2 + O2 → 2H2O.
b) 2KNO3 → 2KNO2 + O2.
c) NH4NO2 → N2 + 2H2O.
d) Fe2O3 + 2Al → 2Fe + Al2O3.
Gợi ý đáp án
Chất khử và chất oxi hóa trong các phản ứng sau là:
![]() \(a) 2{\mathop H\limits^0 _2} + \mathop {{O_2}}\limits^0 \to 2{\mathop H\limits^{ + 1} _2}\mathop O\limits^{ - 2}\)
\(a) 2{\mathop H\limits^0 _2} + \mathop {{O_2}}\limits^0 \to 2{\mathop H\limits^{ + 1} _2}\mathop O\limits^{ - 2}\)
Chất khử: H2, chất oxi hóa là O2
![]() \(b)\mathop {2KN}\limits^{ + 5} {\mathop O\limits^{ - 2} _{3} } \to 2\mathop {KN{O_2}}\limits^{ + 3} + {\mathop O\limits^0 _2}\)
\(b)\mathop {2KN}\limits^{ + 5} {\mathop O\limits^{ - 2} _{3} } \to 2\mathop {KN{O_2}}\limits^{ + 3} + {\mathop O\limits^0 _2}\)
KNO3 vừa là chất oxi hóa, vừa là chất khử
 \(c)\mathop {\mathop N\limits^{ - 3} {H_4}\mathop N\limits^{ + 3} }\limits^{} {\mathop O\limits^{} _3} \to \mathop {{N_2}}\limits^0 + {H_2}\mathop O\limits^{}\)
\(c)\mathop {\mathop N\limits^{ - 3} {H_4}\mathop N\limits^{ + 3} }\limits^{} {\mathop O\limits^{} _3} \to \mathop {{N_2}}\limits^0 + {H_2}\mathop O\limits^{}\)
NH4NO2 vừa là chất oxi hóa, vừa là chất khử.
![]() \(d) {\mathop {Fe}\limits^{ + 3} _2}{\mathop O\limits^{} _3} + 2\mathop {Al}\limits^0 \to \mathop {2Fe}\limits^0 + {\mathop {Al}\limits^{ + 3} _2}\mathop {{O_3}}\limits^{}\)
\(d) {\mathop {Fe}\limits^{ + 3} _2}{\mathop O\limits^{} _3} + 2\mathop {Al}\limits^0 \to \mathop {2Fe}\limits^0 + {\mathop {Al}\limits^{ + 3} _2}\mathop {{O_3}}\limits^{}\)
Câu 8
Dựa vào sự thay đổi số oxi hóa, hãy cho biết vai trò các chất tham gia trong các phản ứng oxi hóa – khử sau:
a) Cl2 + 2HBr → 2HCl + Br2.
b) Cu + 2H2SO4 → CuSO4 + SO2 + 2H2O.
c) 2HNO3 + 3H2S → 3S + 2NO + 4H2O.
d) 2FeCl2 + Cl2 → 2FeCl3.
Gợi ý đáp án
Vai trò các chất trong các phản ứng oxi hóa – khử sau là:
a) ![]() \(\begin{matrix} 0 \\ Cl_{2} \\ \end{matrix} +\begin{matrix} -1 \\ 2HBr \\ \end{matrix}\)→
\(\begin{matrix} 0 \\ Cl_{2} \\ \end{matrix} +\begin{matrix} -1 \\ 2HBr \\ \end{matrix}\)→ ![]() \(\begin{matrix} -1 \\ HCl \\ \end{matrix} +\begin{matrix} 0 \\ Br_{2} \\ \end{matrix}\)
\(\begin{matrix} -1 \\ HCl \\ \end{matrix} +\begin{matrix} 0 \\ Br_{2} \\ \end{matrix}\)
Chất oxi hóa là Cl2, chất khử là Ba-1 (trong HBr)
b) ![]() \(\begin{matrix} 0 \\ Cu \\ \end{matrix} +\begin{matrix} +6 \\ 2H_{2} SO_{4} \\ \end{matrix}\) →
\(\begin{matrix} 0 \\ Cu \\ \end{matrix} +\begin{matrix} +6 \\ 2H_{2} SO_{4} \\ \end{matrix}\) → ![]() \(\begin{matrix} +2 \\ CuSO_{4} \\ \end{matrix} +\begin{matrix} +4 \\ SO_{2} \\ \end{matrix} +\begin{matrix} \\ H_{2} O \\ \end{matrix}\)
\(\begin{matrix} +2 \\ CuSO_{4} \\ \end{matrix} +\begin{matrix} +4 \\ SO_{2} \\ \end{matrix} +\begin{matrix} \\ H_{2} O \\ \end{matrix}\)
Chất oxi hóa là S+6 tron H2SO4, chất khử là Cu
![]() \(c)\mathop {2HN}\limits^{ + 5} {\mathop O\limits^{ - 2} _3} + 3{H_2}\mathop S\limits^{ - 2} \to 3S + 2\mathop {NO}\limits^{ + 2} + 4{H_2}O\)
\(c)\mathop {2HN}\limits^{ + 5} {\mathop O\limits^{ - 2} _3} + 3{H_2}\mathop S\limits^{ - 2} \to 3S + 2\mathop {NO}\limits^{ + 2} + 4{H_2}O\)
Chất oxi hóa là N+5 (trong HNO3), chất khử là S-2 (trong H2S)
 \(d){\mathop {2FeCl}\limits^{ + 2} _2} + {\mathop {Cl}\limits^0 _2} \to 2{\mathop {\mathop {Fe}\limits^{ + 3} \mathop {Cl}\limits^{ - 1} }\limits^{} _3}\)
\(d){\mathop {2FeCl}\limits^{ + 2} _2} + {\mathop {Cl}\limits^0 _2} \to 2{\mathop {\mathop {Fe}\limits^{ + 3} \mathop {Cl}\limits^{ - 1} }\limits^{} _3}\)
Chất oxi hóa là Cl2, chất khử là Fe+2 (trong FeCl2)
Câu 9
Cân bằng các phương trình phản ứng oxi hóa – khử sau đây bằng phương pháp thăng bằng electron và cho biết chất khử, chất oxi hóa ở mỗi phản ứng:
a) Al + Fe3O4 → Al2O3 + Fe
b) FeSO4 + KMnO4 + H2SO4 → Fe2(SO4)3 + MnSO4 + K2SO4 + H2O
c) FeS2 + O2 → Fe2O3 + SO3
d) KClO3 → KCl + O2
e) Cl2 + KOH → KCl + KClO3 + H2O
Gợi ý đáp án
Cân bằng các phương trình phản ứng oxi hóa – khử:
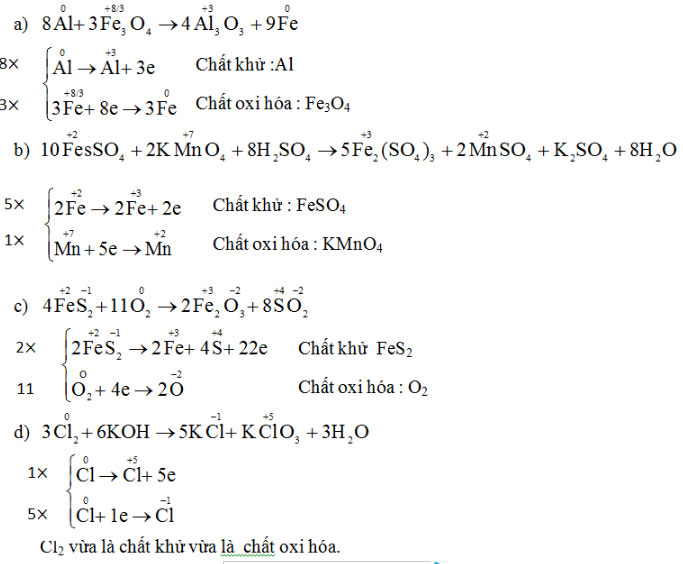
Câu 10
Có thể điều chế MgCl2 bằng:
- Phản ứng hóa hợp.
- Phản ứng thế.
- Phản ứng trao đổi.
Gợi ý đáp án
Điều chế MgCl2 bằng:
Phản ứng hóa hợp: Mg + Cl2 → MgCl2
Phản ứng thế: Mg + CuCl2 → MgCl2 + Cu
Phản ứng trao đổi: Mg(OH)2 + 2HCl → MgCl2 + 2H2O
Câu 11
Cho những chất sau: CuO, dung dịch HCl, H2, MnO2.
a) Chọn từng cặp trong những chất đã cho để xảy ra phản ứng oxi hóa – khử và viết phương trình phản ứng.
b) Cho biết chất oxi hóa, chất khử, sự oxi hóa và sự khử trong những phản ứng hóa học nói trên.
Gợi ý đáp án
a) Những cặp chất xảy ra phản ứng oxi hóa - khử:
(1) Cu+2O + Ho2 ![]() \(\overset{t^{\circ } }{\rightarrow}\) oCu + H+12O
\(\overset{t^{\circ } }{\rightarrow}\) oCu + H+12O
(2) MnO2 + 4HCl → MnCl2 + Cl2 + 2H2O
b) Trong phản ứng (1):
Nguyên tử hiđro nhường electron là chất khử, sự nhường electron của H2 được gọi là sự oxi hóa nguyên tử hiđro.
Ion Cu nhận electron, là chất oxi hóa. Sự nhận electron của ion đồng được gọi là sự khử ion đồng.
Trong phản ứng (2):
Ion Clo nhường electron là chất khử. Sự nhường electron của Cl- được gọi là sự oxi hóa ion Clo.
Ion Mn nhận electron là chất oxi hóa. Sự nhận electron của ion Mn được gọi là sự khử ion Mn.
Câu 12
Hòa tan 1,39g muối FeSO4.7H2O trong dung dịch H2SO4 loãng. Cho dung dịch này tác dụng với dung dịch KMnO4 0,1M. Tính thể tích dung dịch KMnO4 tham gia phản ứng.
Gợi ý đáp án
Phương trình hóa học của phản ứng:
10FeSO4 + 2KMnO4 + 8H2SO4 → 5Fe2(SO4)3 + K2SO4 + 2MnSO4 + 8H2O.
nFeSO4.7H2O = 1,39 / 278 = 0,005 mol = nFeSO4.
nKMnO4= 2nFeSO4 = 0,01 mol.
Vdd KMnO4 = 0,001 / 0,1 = 0,01 (lit).
Theo Nghị định 147/2024/ND-CP, bạn cần xác thực tài khoản trước khi sử dụng tính năng này. Chúng tôi sẽ gửi mã xác thực qua SMS hoặc Zalo tới số điện thoại mà bạn nhập dưới đây:
Chủ đề liên quan
Có thể bạn quan tâm
-

Văn mẫu lớp 7: Tóm tắt truyện ngắn Cuộc chia tay của những con búp bê (7 mẫu)
-

Bộ đề thi học kì 2 môn Lịch sử - Địa lý lớp 5 năm 2024 - 2025 (Sách mới)
-

Biên bản lựa chọn sách giáo khoa lớp 3
-

Bộ đề ôn thi học kì 2 môn Ngữ văn 8 năm 2023 - 2024 (Sách mới)
-

Bộ đề thi học kì 2 môn Tiếng Anh 6 năm 2024 - 2025 sách Kết nối tri thức với cuộc sống
-

Bộ đề thi học kì 2 môn Vật lý lớp 10 năm 2024 - 2025 (Sách mới)
-

Văn mẫu lớp 10: Phân tích mâu thuẫn giữa Tấm và mẹ con Cám
-

Phân tích về bài thơ Chốn quê của Nguyễn Khuyến
-

Bộ đề thi học kì 2 môn Tiếng Việt 5 năm 2024 - 2025 sách Kết nối tri thức với cuộc sống
-

Bài phát biểu tổng kết công tác hội phụ nữ năm 2022
Mới nhất trong tuần
-

Địa lí 10 Bài 32: Thực hành Viết báo cáo tìm hiểu một vấn đề công nghiệp
1.000+ -

Chuyên đề Nguyên tố nhóm halogen
100+ -

Chuyên đề Tốc độ phản ứng
100+ -

Chuyên đề Năng lượng hóa học
100+ -

Chuyên đề Phản ứng oxi hóa - khử
100+ -

Chuyên đề Liên kết hóa học
100+ -

Chuyên đề Bảng tuần hoàn các nguyên tố hóa học và định luật tuần hoàn
100+ -
Chuyên đề Cấu tạo nguyên tử
100+ -

Hóa học 10 Bài 8: Định luật tuần hoàn. Ý nghĩa của bảng tuần hoàn các nguyên tố hóa học
1.000+ -

Hóa học 10 Bài 7: Xu hướng biến đổi thành phần và một số tính chất của hợp chất trong một chu kì
1.000+






 Toán 10 Kết nối tri thức
Toán 10 Kết nối tri thức
 Toán 10 Chân trời sáng tạo
Toán 10 Chân trời sáng tạo
 Toán 10 Cánh Diều
Toán 10 Cánh Diều
 Soạn văn 10 Chân trời sáng tạo
Soạn văn 10 Chân trời sáng tạo
 Soạn văn 10 Cánh Diều
Soạn văn 10 Cánh Diều
 Soạn văn 10 Kết nối tri thức
Soạn văn 10 Kết nối tri thức
 Tiếng Anh 10 Global Success
Tiếng Anh 10 Global Success
 Tiếng anh 10 Friends Global
Tiếng anh 10 Friends Global
 Tiếng Anh 10 Explore New Worlds
Tiếng Anh 10 Explore New Worlds